热点聚焦
抗Aβ疗法的生死等待
- 分类: 热点聚焦
- 作者: 黄荣
- 发布时间: 2020-12-04 13:15
虽然阿尔茨海默症被发现以来已逾百年,但其发病原因至今未有定论。随着人口老龄化进程的加速,阿尔茨海默症患病人数逐年增加。然而该领域新药研发屡屡遭遇失败,再加上阿尔茨海默症治疗的巨大未满足需求,寻找缓解阿尔茨海默症认知下降或阻止其进展的药物,如今已成为生物制药行业关注的重点领域之一。
1、 Aducanumab能否开启新时代?
在阿尔茨海默症领域,百健和卫材联合开发的抗β-淀粉样蛋白(Aβ)单克隆抗体Aducanumab无疑是近期业内关注的焦点项目之一。
继11月3日欧洲药品管理局(EMA)确认接受Aducanumab的上市授权申请(MAA),11月4日美国食品药品管理局(FDA)内部审查意见给出了积极意见之后,11月6日该项目终于迎来上市前最为关键的事件——FDA外周和中枢神经系统药物咨询委员会会议。
在FDA针对Aducanumab召开的此次外部专家咨询委员会会议上,专家们对该药物的临床研究证据问题进行了投票表决,几乎所有外部专家都给出了负面评价。此外,外部专家还直言FDA欠缺专业性,认为之前FDA给出的积极内部审查意见令他们感到费解。
FDA咨询委员会提供非约束性建议,仅供FDA审议。根据咨询委员会表达的意见和所提供的数据,FDA将继续进行审评,并在2021年3月7日之前决定是否批准Aducanumab生物制品上市申请(BLA)。
受到近期Aducanumab影响,百健股价在FDA内部审查意见给出了积极意见之后暴涨近44%,而在专家咨询委员会给出负面评价后却又狂跌28%。
无论最终结果如何,Aducanumab现在已是近20年来最接近FDA批准的阿尔茨海默症药物,也是1991年提出β-淀粉样蛋白假说之后该靶点进展最快的药物。
2、后继者:新技术带来新希望
尽管β-淀粉样蛋白抗体屡遭失败,但还有众多的生物制药公司开始在阿尔茨海默症对其同类项目进行早期阶段的测试。
其中拥有最多β-淀粉样蛋白项目的礼来在FDA内部审查意见给出Aducanumab积极意见之后股票也随之上涨了13%,大概是因为希望其领先的阿尔茨海默症项目Solanezumab能够取得同样肯定。
礼来的Solanezumab比大多数竞争项目进展更快,在一项名为A4的Ⅲ期临床试验研究中,主要是针对大脑中存在β-淀粉样蛋白斑块证据,但还未进展为阿尔茨海默症的老年人。A4试验目的是为研究Solanezumab对极早期阿尔茨海默症的影响。该研究本来于2014年2月启动,时间为期三年。2017年6月,由于礼来领导层的变化,A4试验时间进行延长,试验结果计划于2023年初公布。
一项名为DIAN-TU的随机、双盲、安慰剂对照的Ⅱ/Ⅲ期阿尔茨海默病临床试验,招募490位显性遗传阿尔茨海默症患者(ADAD),分别使用礼来的Solanezumab、罗氏的Gantenerumab和安慰剂。今年2月公布的数据来自对194位患者平均跟踪5年、最长7年的观察,结果两个药物都未能改善认知功能,错过试验一级终点。
尽管如此,并没有阻止2家公司对各自项目的信心。罗氏正在对Gantenerumab开展2项Graduate 1/Graduate 2的Ⅲ期临床试验,分别招募了1000名阿尔茨海默症早期患者,并计划于2022年完成。在百健和礼来股票大涨的同期,罗氏的股票当天收盘也上涨5%。
在早期开发项目中,针对β-淀粉样蛋白的方法略有不同。例如,罗氏有一种名为RG6102的Gantenerumab的“脑穿梭”制剂,据悉可以增加大脑中的抗体浓度。
同时,礼来的N3pG抗体Donanemab可与pGlu-β-淀粉样蛋白结合,后者参与了毒性低聚物的形成。礼来希望在明年年初报告该项目Ⅱ期Trailblazer-Alz试验的数据。
礼来还拥有新一代N3pG抗体,目前正在进行Ⅰ期测试,该方法不会诱导人体产生抗药物抗体。抗药物抗体可能降低药物疗效,或者引起过敏反应,甚至威胁生命。
百健、礼来和罗氏是开发β-淀粉样蛋白抗体药物的领航者,而进展最快的Aducanumab如获得FDA批准,无疑将会迎来β-淀粉样蛋白药物的繁荣期。
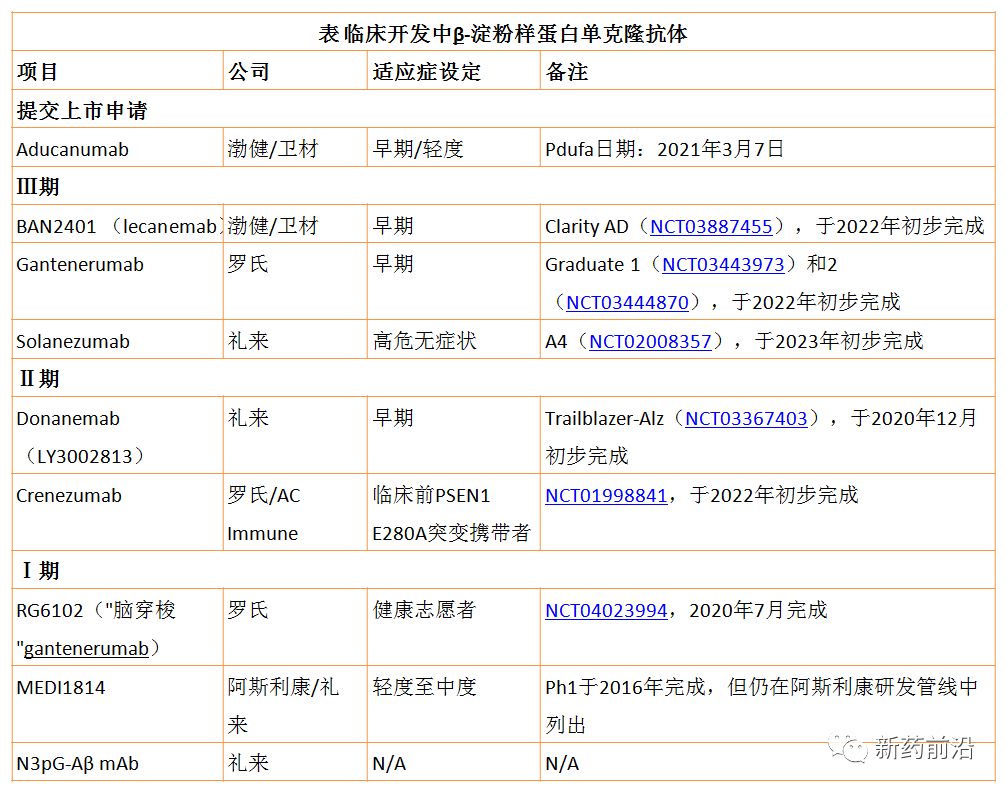
来源:新药前沿